 |
|
Стволовые клетки (обзор)Существование стволовых клеток в некоторых тканях сначала было предсказано теоретически. Вильсон (Е. В. Wilson, 1896) еще в первом издании своей книги <Клетка в развитии и наследственности> предположил существование стволовых клеток, обеспечивающих поддержание сперматогенеза. А.А. Максимов в 1908 г. постулировал существование стволовой кроветворной клетки. Исследования в области стволовых клеток крови активно развивались с начала 50-х годов. Изучение кинетики клеточных популяций в быстро обновляющихся тканях, таких как кровь, эпителий кишечника, эпидермис, показало, что в них происходит очень быстрая смена дифференцированных клеток. Так, в процессе гемопоэза у человека ежечасно продуцируется, и, следовательно, разрушается 1 миллиард эритроцитов и 100 миллионов лейкоцитов. Такое количество специализированных клеток, естественно, может быть обеспечено только за счет пролиферации некоторого числа самоподдерживающихся клеток, которые стали рассматривать как стволовые (схема).Основные элементы концепции стволовых клеток были разработаны при изучении системы гемопоэза и в дальнейшем распространены на другие быстро обновляющиеся ткани, в частности эпидермис. В последнее время появились сообщения о том, что стволовые клетки присутствуют и в таких органах как центральная нервная система, где ранее их существование не предполагали. Поведение и характерные черты стволовых клеток во многом зависят от физиологических особенностей тех тканей, в которых они находятся. Самое существенное свойство стволовых клеток заключается в том, что они могут самоподдерживаться в течение длительного времени и при этом производить дифференцированные клетки, которые выполняют в организме специфические функции.
Схема
I - компартмент стволовых клеток; А - длительно самоподдерживающаяся стволовая клетка, которая при редких делениях производит стволовые клетки В, также самоподдерживающиеся ограниченное время и производящие транзитор-ные клетки; II - компартмент транзиторных клеток, которые активно размножаются, но при некоторых условиях могут вернуться в компартмент I, что показано пунктирной стрелкой для клетки С; III - компартмент дифференцированных клеток, которые выполняют определенные функции, не размножаются, но в некоторых тканях сохраняют способность к пролиферации. Биологическая значимость стволовых клеток заключается в том, что они играют ведущую роль в организации многоклеточных организмов и являются центральным элементом структурно-функциональных единиц тканей и органов. По мнению Вейсмана, стволовые клетки - это не только единицы организации ткани, ответственные за развитие и поддержание гомеостаза и регенерацию тканей и органов, но и единицы эволюции. Пролиферативный потенциал стволовых клеток в обновляющихся тканях очень велик и продолжительность жизни популяции стволовых клеток может значительно превосходить продолжительность жизни организма, что было показано путем последовательного пассирования гемопоэтических стволовых клеток мышам, получившим летальную дозу облучения. Такие же данные существуют для стволовых клеток кожи. Так, у лабораторных мышей, продолжительность жизни которых достигает 3 лет, эпидермальные стволовые клетки делятся за этот период времени около 100 раз. Крон показал, что можно серийно трансплантировать до 5 раз кожные лоскуты молодым животным, общая продолжительность жизни этих лоскутов составляла от 4,5 до 5 лет, причем в конце экспериментов состояние лоскутов было еще вполне удовлетворительным. Эти данные позволяют считать, что продолжительность жизни стволовых клеток эпидермиса может быть значительно больше, чем продолжительность жизни организма в целом. Имеются данные, согласно которым с возрастом число стволовых клеток у людей уменьшается, но все еще остается на достаточно высоком уровне. В то же время продолжительность жизни отдельных стволовых клеток может быть ограниченной. Некоторые стволовые клетки функционируют только в определенном временном интервале. К их числу можно отнести эмбриональные и фетальные стволовые гемопоэтические клетки. Герминативные стволовые клетки в яичниках млекопитающих самоподдерживаются во время эмбриогенеза, и уже к моменту рождения продукция ооцитов заканчивается. Таким образом, не все стволовые клетки, образовавшиеся в эмбриональном периоде развития, сохраняются во взрослом организме. Поведение стволовых клеток во многом определяется свойствами тех тканей, в которых они находятся и которые они поддерживают. Обычно считается, что стволовые клетки обладают "неограниченной" способностью к самоподдержанию, то есть могут сохранять свойства и пролиферативный потенциал на протяжении всей жизни организма. Однако в быстро обновляющихся тканях существует сложная структура клеточной популяции, в которой представлены:
Изучение судьбы радиоактивно меченных кератиноцитов в эпидермисе мыши показывает достаточно быстрое исчезновение метки из тканей, что говорит о высокой пролиферативной активности клеток. Однако некоторое число меченых кератиноцитов может сохраняться в состоянии покоя в течение нескольких месяцев. В волосяных фолликулах также присутствуют стволовые эпидермальные клетки, которые могут длительное время находиться в состоянии покоя. Длительное сохранение метки (то есть пребывание клетки в состоянии покоя) рассматривают как один из характерных признаков стволовых клеток. Разработка методов культивирования in vitro позволяет определить способность отдельных кератиноцитов образовывать клоны, состоящие из потомков этих клеток, и использовать этот показатель для выявления стволовых (клоногенных) клеток. Баррандон и Грин изучили способность кератиноцитов разного размера образовывать клоны в культуре клеток. Было выявлено, что мелкие кератиноциты дают начало клонам с большой частотой, более крупные клетки дают клоны с меньшей частотой, и, наконец, еще более крупные клетки никогда не образуют клоны. Кератиноциты, выделенные из эпидермиса, могут образовывать клоны, если их диаметр меньше 11 мкм, но они уже необратимо комитированы к дифференциации (запрограммированы), если их диаметр составляет 12 мкм или более. Изучение культур кератиноцитов также показало значительную гетерогенность их популяции. Баррандон и Грин установили, что кератиноциты человека, выделенные из эпидермиса, могут образовывать клоны, которые морфологически гетерогенны, значительно различаются по пролиферативному потенциалу и могут быть подразделены на три группы. Голо-клоны (holo - полный) образованы мелкими округлыми базальными клетками, они имеют максимальную способность к пролиферации: за 12 дней они производят от 20 до 50 тыс. клеток. В целом, голоклоны могут проходить до 100 генераций. Параклоны (para - около) содержат исключительно клетки с низким пролиферативным потенциалом: они проходят не более 15 генераций, после чего переходят к терминальной дифференциации. И, наконец, мероклоны (mero - часть) содержат клетки с разным пролиферативным потенциалом и представляют собой промежуточную стадию между голоклонами и параклонами. Считается, что голоклоны образованы стволовыми клетками. Можно также предположить, что мероклоны образованы короткоживущими стволовыми и транзиторными клетками.
Ниша стволовых клетокСтволовые клетки не существуют в организме сами по себе, они находятся в определенном микроокружении, которое обычно обозначают термином ниша. В настоящее время этот термин используется для обозначения совокупности факторов, обеспечивающих жизнеспособность и самовоспроизведение стволовых клеток и дифференциацию дочерних транзиторных клеток. Среди этих факторов следует упомянуть наличие базальной мембраны, молекул внеклеточного матрикса и присутствие соседних клеток, продуцирующих факторы роста и другие регуляторные молекулы (рис.).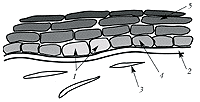 Ниша активно участвует в регуляции
пролиферации и дифференциации стволовых клеток, она обеспечивает
самоподдержание стволовых клеток и длительное их пребывание в состоянии
покоя. Стволовые клетки прочно закреплены в нише молекулами адгезии, в
частности интегринами. В то же время свободные стволовые клетки могут
находить путь в соответствующую нишу благодаря хемотаксису. Ниши являются
частью структурно-функциональных единиц, из которых состоят ткани.
Ниша активно участвует в регуляции
пролиферации и дифференциации стволовых клеток, она обеспечивает
самоподдержание стволовых клеток и длительное их пребывание в состоянии
покоя. Стволовые клетки прочно закреплены в нише молекулами адгезии, в
частности интегринами. В то же время свободные стволовые клетки могут
находить путь в соответствующую нишу благодаря хемотаксису. Ниши являются
частью структурно-функциональных единиц, из которых состоят ткани.
Ниша стволовых клеток может оставаться свободной и в дальнейшем ее могут занять новые клетки. Пустые ниши могут существовать независимо от стволовых клеток и при трансплантации в них стволовых клеток обеспечивать их нормальное функционирование. Одно из назначений ниши в тканях взрослого организма заключается в ограничении пролиферации стволовых клеток только необходимостью поддерживать тканевой гомеостаз. Другое назначение ниши - создание условий для максимальной защищенности стволовых клеток от внешних воздействий. Например, стволовые клетки эпителия кишечника находятся в нижней части крипт (рис. 2), в волосяном фолликуле стволовые клетки локализуются под сальной железой (рис. 3), стволовые клетки роговицы - в области лимба. Переход стволовых клеток в состояние покоя также повышает их устойчивость к внешним воздействиям.
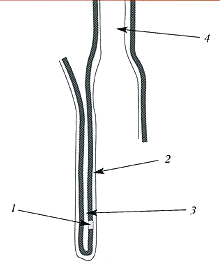
Рис. 2. Ниши стволовых клеток, крипта тонкого кишечника: 1 - стволовые клетки; 2 - базальная мембрана; 3 - крипта; 4 - ворсинка
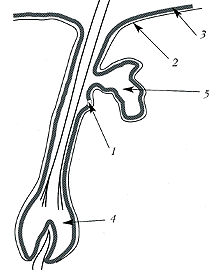
Рис. 3. Ниши стволовых клеток, волосяной фолликул: 1 - стволовые клетки
наружного волосяного влагалища ниже сальной железы; 2 - базальная мембрана;
3 - эпидермис; 4 - волосяная луковица; 5 - сальная железа
Для самоподдержания стволовые клетки должны получать от своего микроокружения (ниши) определенные сигналы. Например, для поддержания эмбриональных стволовых клеток мыши в недифференцированном состоянии in vitro необходим фактор ингибирования лейкемии (LIF). Внутриклеточные сигналы также необходимы для поддержания неограниченной пролиферации стволовых клеток. Для поддержания плюрипотентности и предотвращения дифференциации эмбриональных стволовых клеток необходима экспрессия транскрипционного фактора Nanog. В результате деления стволовые клетки дают начало дочерним клеткам с коротким клеточным циклом. Дочерние клетки благодаря нескольким последовательным делениям создают большой компартмент (популяцию) транзиторных клеток, которые затем превращаются в дифференцированные клетки, выполняющие специфические функции в организме. Образование большого количества дифференцированных клеток обеспечивается именно за счет размножения транзиторных клеток при малом числе делений стволовых клеток. Это позволяет уменьшить риск генетических нарушений, которые могут произойти в процессе репликации и пролиферации стволовых клеток, поскольку именно с генетическими нарушениями стволовых клеток связан неопластический рост. Генетические нарушения в транзиторных клетках представляют меньшую опасность, поскольку эти клетки, как правило, прекращают пролиферацию и дифференцируются. Длительное время существовало убеждение, что транзиторные клетки необратимо выходят из компартмента стволовых клеток, однако постепенно стали появляться данные, свидетельствующие о том, что между стволовыми и транзиторными клетками нет резкой границы, а скорее имеется постепенный переход. После того как стволовые клетки в результате деления дают начало транзиторным клеткам, последние еще некоторое время могут сохранять свойства стволовых клеток. Поттен называет их потенциальными стволовыми клетками и считает, что в норме они относятся к транзиторной популяции, но при определенных условиях, например, гибели пред существующих стволовых клеток, могут заместить последние. Представляют интерес экспериментальные данные относительно большой пластичности транзиторных клеток. Транзиторные клетки эпителия роговицы находятся в ее центральной части и легко могут быть отделены от стволовых клеток, которые локализованы в области лимба. Было установлено, что транзиторные клетки эпителия роговицы кролика могут быть перепрограммированы при взаимодействии с дермой эмбрионов мыши (дорсальной, верхней губы и подошвы). Полученные результаты показывают, что клетки роговицы взрослого животного отвечают на специфические стимулы эмбриональной дермы. Сначала появляется новый базальный слой клеток, в котором не экспрессируются кератины роговицы, а затем появляются пилосебацейные единицы, или потовые железы, в зависимости от типа дермы, и наконец в верхних слоях клеток появляется экспрессия кератинов эпидермального типа. Таким образом, происходит перепрограммирование клеток роговицы.
Пролиферация стволовых клетокМногие типы стволовых клеток способны длительное время находиться в состоянии покоя, в результате чего они редко делятся и имеют поэтому большую продолжительность клеточного цикла. Это относится, например, к стволовым клеткам кожи и крови. В эпидермисе мыши можно выделить как минимум две субпопуляции клеток, различающихся по скорости пролиферации. Большая по размеру субпопуляция включает активно пролиферирующие транзиторные клетки с более коротким клеточным циклом. Средняя продолжительность клеточного цикла этой субпопуляции составляет около 120 часов, а второй субпопуляции стволовых клеток - около 200 часов. Сложность определения параметров клеточного цикла стволовых клеток заключается в том, что многие из них выходят из цикла в состояние покоя на длительный срок. Моррис и Поттен установили, что в дорсальном эпидермисе и волосяных фолликулах взрослых мышей стволовые клетки могут находиться в покое в течение 8-10 недель.Благодаря такой структуре клеточной популяции в организме удается поддерживать гомеостаз эпидермиса за счет очень небольшого числа делений стволовых клеток. Транзиторные клетки проходят несколько делений, находясь в базальном слое эпидермиса, прежде чем дают начало комитированным клеткам, которые переходят в супрабазальные слои эпидермиса, выходят из клеточного цикла и терминально дифференцируются. Это обеспечивает быстрое обновление эпидермиса при относительно небольшом числе делений стволовых клеток. В других случаях стволовые клетки могут иметь очень короткий цикл. Например, пролиферативный цикл стволовых клеток крипты тонкого кишечника равен приблизительно 24 часам. В общем, можно сказать, что в тканях взрослого организма стволовые клетки пролиферируют сравнительно медленно, но это не является обязательным свойством стволовых клеток. Экспериментально определить продолжительность пребывания некоторых стволовых клеток в состоянии покоя трудно, однако имеющиеся данные позволяют заключить, что некоторые стволовые клетки могут находиться в покое исключительно длительное время. Учитывая пролиферативные характеристики, можно представить себе следующую иерархию стволовых и транзиторных клеток. В ткани имеется некоторое число стволовых клеток, которые находятся в глубоком покое и делятся редко. Лишь когда внешние воздействия или общий недостаток стволовых клеток вызывают их мобилизацию, стволовые клетки начинают пролиферировать. Кроме того, имеется достаточно много активно пролиферирующих, обычно короткоживущих стволовых клеток, которые образуют большое число транзиторных клеток, производящих в свою очередь дифференцированные клетки (схема).
Асимметричное деление стволовых клетокОдна из важных характеристик стволовых клеток заключается в том, что они продуцируют дифференцированные клетки и в то же время самоподдерживаются. Теоретически возможны два способа реализации такого поведения стволовых клеток. Во-первых, стволовая клетка может вступить в "асимметричный митоз", в результате которого возникнут две дочерние клетки с разными свойствами: одна из них останется стволовой, а другая - приступит к дифференциации. Во-вторых, стволовая клетка может делиться симметрично, но в дальнейшем, попадая в разное микроокружение, дочерние клетки могут пойти по разным путям развития. Осгуд первым предположил, что транзиторные клетки, способные в дальнейшем к дифференциации, образуются в результате асимметричного деления стволовых клеток, но в тех случаях, когда по какой-либо причине возникает дефицит стволовых клеток, они могут делиться симметрично, восполняя число стволовых клеток. Таким образом, в зависимости от ситуации стволовые клетки могут выбирать между симметричным и асимметричным делением.В ряде случаев асимметричность деления хорошо прослеживается, например, при делении стволовых клеток у Drosophila. В стволовых герминативных клетках яичника дрозофилы асимметричное деление определяется клеточной органеллой спектросомой, которая ассоциирована с одним из полюсов митотического веретена и обеспечивает связь стволовой клетки с базальной мембраной гермария. У млекопитающих асимметричность деления стволовых клеток кожи не обнаружена, но в эпителии пищевода человека митотическое веретено расположено перпендикулярно базальной мембране, и поэтому одна дочерняя клетка остается прикрепленной к мембране, а другая оказывается в супрабазальном положении.
Дифференциация стволовых клетокЧасто возникает вопрос о степени дифференцированности стволовых клеток. Стволовые клетки взрослого организма менее дифференцированы, чем специализированные клетки, которым они дают начало, но более дифференцированы, чем их предшественники из эмбриональных тканей. Поэтому правильнее было бы считать, что дифференциация стволовых клеток соответствует тому микроокружению (нише), в котором они находятся.Стволовые клетки способны продуцировать дочерние клетки, которые в дальнейшем дают начало различным линиям дифференцированных клеток. Моррисон с соавт. считает, что стволовые клетки способны производить все дифференцированные клетки, которые возможны в конкретной ткани и в конкретное время. Обычно стволовые клетки производят дочерние клетки, которые способны дифференцироваться в разных направлениях, давать разные линии клеток, что обозначается термином "мультипотентность". Например, гемато-поэтические стволовые клетки дают начало всем линиям клеток крови. Но могут быть стволовые клетки, которые дифференцируются только в одном направлении (монопотентность), например герминативные стволовые клетки, производящие гаметы одного пола.
Стволовые клетки в онтогенезеВ начале 80-х годов из внутренней клеточной массы бластоцисты мыши удалось получить линии эмбриональных стволовых клеток. В отличие от "взрослых" (постнатальных) стволовых клеток, эмбриональные стволовые клетки обладают тотипотентностью, то есть могут дифференцироваться и давать начало линиям клеток, относящимся к трем зародышевым листкам и характеризующимся нейральными, гематопоэтическими и другими маркерами.В онтогенезе стволовые клетки возникают в определенный временной промежуток и часто формируются в одних участках организма, а выполняют свою функцию - в других, в связи с чем наблюдается миграция стволовых клеток в новое микроокружение. Так, первые гематопоэтические стволовые клетки мыши появляются вне эмбриона в желточном мешке, на следующем этапе развития организма стволовые кроветворные клетки обнаруживаются в области эмбриона, которая называется аорта-гонадамезонефрос, затем органом кроветворения становится печень и, наконец, у взрослого организма кроветворение происходит в трубчатых костях и селезенке. Волосяные фолликулы часто рассматривают как резервуар эпидермальных стволовых клеток, поскольку они могут давать начало эпидермальным кератиноцитам и нескольким линиям кератиноцитов волосяного фолликула. Образование волосяных фолликулов происходит только в определенный временной промежуток онтогенеза, после чего они в редких случаях и у некоторых видов млекопитающих могут возникать заново.
Маркеры стволовых клеток Стволовые клетки обладают некоторыми характерными морфологическими
признаками, типичными для мало дифференцированных "примитивных" клеток.
Например, стволовые клетки эпидермиса ладони имеют небольшие размеры и
относительно большое ядерно-цитоплазматическое отношение, их поверхность
покрыта большим количеством микроворсинок, среди которых имеются вкрапления
десмосом. Цитоплазма заполнена свободными рибосомами, митохондриями и
меланосомами. Кроме того, в этих клетках мало кератиновых филаментов и
ядерный хроматин распределен диффузно (фото).
Стволовые клетки обладают некоторыми характерными морфологическими
признаками, типичными для мало дифференцированных "примитивных" клеток.
Например, стволовые клетки эпидермиса ладони имеют небольшие размеры и
относительно большое ядерно-цитоплазматическое отношение, их поверхность
покрыта большим количеством микроворсинок, среди которых имеются вкрапления
десмосом. Цитоплазма заполнена свободными рибосомами, митохондриями и
меланосомами. Кроме того, в этих клетках мало кератиновых филаментов и
ядерный хроматин распределен диффузно (фото).
Фото. Электронно-микроскопическое изображение эпидермальных кератиноцитов
человека, имеющих морфологию, характерную для стволовых клеток: Я - ядро;
MX - митохондрия; XT - хроматин; МС - меланосома; PC - рибосомы
Однако морфологические признаки не позволяют провести четкую границу между стволовыми и транзиторными клетками. Поэтому для идентификации стволовых клеток нужны иные маркеры. Поиски маркеров предпринимаются для выделения стволовых клеток в чистом виде, что, с одной стороны, позволяет изучать их биологию, а с другой - использовать в клинической практике. Лучше всего изучены маркеры гемопоэтических стволовых клеток. Известны маркеры для стволовых и прогениторных нейральных клеток, например Musashi 1. Одним из характерных маркеров эмбриональных стволовых клеток является Oct4. Много исследований было посвящено иммунофлуоресцентному выявлению маркеров эпидермальных стволовых клеток. Среди предложенных маркеров можно отметить кератин 19, интегрин b1, внутриклеточный белок рбЗ. Изучение экспрессии маркеров показало, что между стволовыми и транзиторными клетками трудно провести четкую границу, поэтому для выделения эпидермальных стволовых клеток используют несколько маркеров. Исследования показали также, что предполагаемые стволовые клетки экспрессируют высокий уровень интегрина аб, входящего в комплекс десмосом, и низкий уровень маркера клеточной поверхности (рецептор трансферрина), который распознается монокло-нальными антителами 10G7. Было предположено, что клетки с фенотипом a6bn10G7dim (яркая флуоресценция аб и тусклая флуоресценция 10G7) представляют собой эпидер-мальные стволовые клетки, составляющие около 8% эпидермальных клеток, и проявляют самую высокую способность к регенерации. По другим оценкам, фракция стволовых эпидермальных клеток составляет от 1 до 10% клеток базального слоя. Точная оценка фракции стволовых клеток затруднена методически, а также ввиду того, что часть транзиторных клеток еще сохраняет свойства стволовых клеток. Однако все известные в настоящее время маркеры не позволяют с полной уверенностью отделить стволовые клетки от транзиторных. Как было указано ранее, между этими двумя группами клеток наблюдается постепенный переход.
Гетерогенность популяции стволовых клетокСтволовые клетки каждой ткани оказываются во многих отношениях гетерогенными, что можно рассматривать как генетически обусловленное свойство популяции, обеспечивающее ей устойчивость к неблагоприятным внешним воздействиям. Изучение кроветворения показало, что существуют короткоживущие и долгоживущие гематопоэтические стволовые клетки, то есть некоторые стволовые клетки имеют ограниченную продолжительность жизни, тогда как определенная группа стволовых клеток может сохраняться на протяжении всей жизни организма.Обнаружена функциональная гетерогенность гематопоэтических стволовых клеток по их способности защищать мышей, получивших летальную дозу облучения. Покоящиеся стволовые клетки обладают более высокой защитной способностью, чем активно пролиферирующие клетки. Гетерогенность также наблюдается и в экспрессии маркеров. Например, длительное время считали, что стволовые гематопоэтические клетки обязательно несут маркер CD34+, однако было доказано, что и клетки CD34- также могут быть стволовыми. В коже могут одновременно находиться стволовые клетки, обладающие разным пролиферативным потенциалом.
Пластичность стволовых клетокДолгое время существовало убеждение, что уровень дифференциации стволовых клеток взрослого организма остается неизменным, но постепенно стали появляться сведения о том, что биология стволовой клетки гораздо сложнее, чем предполагалось ранее. Было установлено, например, что стволовые клетки костного мозга способны не только восстанавливать кроветворение, но также находить новые ниши и дифференцироваться в клетки других органов: печени, мозга, скелетных мышц и сердца. Стволовые мезенхимные клетки, выделенные из костного мозга, могут дифференцироваться практически во все типы соматических клеток.В связи с этим было предположено, что стволовые клетки представляют собой не столько конкретные клетки, сколько биологическую функцию. Однако есть авторы, считающие, что такое расширенное толкование феномена стволовых клеток пока еще преждевременно. По-видимому, статус стволовых клеток должен постоянно поддерживаться за счет поступающих в клетки сигналов и синтеза определенных белков. Микроокружение производит сигналы, определяющие поведение стволовых клеток. Например, нейральные стволовые клетки присутствуют в разных отделах мозга, но реализуют эту возможность только клетки, локализованные в определенных участках. В то же время фактор роста фибробластов (FGF-2) может активировать латентные нейральные стволовые клетки из разных участков взрослого мозга. В связи с этим направление дифференциации потомков стволовых клеток может определяться сигналами, которые создаются в каждой конкретной нише. За последнее время увеличилось число сообщений, согласно которым стволовые (или подобные им) клетки могут быть выделены из разнообразных тканей взрослого организма. Причем эти клетки способны мигрировать в поврежденные участки тканей и стимулировать репарацию дефекта либо путем дифференциации в клетки этих тканей, либо путем создания микроокружения, усиливающего репарацию эндогенных стволовых клеток. Проблема пластичности стволовых клеток в настоящее время активно обсуждается.
Использование стволовых клеток в клиникеДля клеточных технологий, которые можно использовать в клинической практике, в первую очередь представляют интерес "взрослые" (постнатальные) стволовые клетки. Существенным моментом является то, что стволовые клетки, например эпидермиса человека, можно длительное время культивировать вне организма и таким образом наращивать большое количество клеток. При этом стволовые клетки сохраняют свой пролиферативный потенциал и могут быть трансплантированы реципиенту.Первый большой успех в использовании клеточных технологий связан с успешной трансплантацией выращенного эпителия на полнослойные раны двум пациентам, один из которых в результате тяжелых ожогов потерял 80%, а другой частично или полностью 40% кожного покрова. Способность стволовых клеток интегрироваться в трехмерные тканевые структуры организма под контролем микроокружения реципиента делает их использование идеальным подходом для цитозаместительной терапии. Первые успехи клеточных технологий были связаны с гистотипическим восстановлением дефектов кожного покрова с помощью тканевой инженерии. Были разработаны трехмерные клеточные конструкции, состоящие из внеклеточного матрикса и аутологичных или аллогенных клеток, названные "живыми эквивалентами дермы и кожи", которые использовали для трансплантации на ожоговые поверхности, длительно незаживающие раны и язвы разной природы. Успешно используются методы тканевой инженерии для лечения ожогов и язв роговицы. Многие исследователи связывают большие перспективы для клинической практики с использованием эмбриональных стволовых клеток. Эмбриональные стволовые клетки можно стимулировать к дифференциации в разные типы клеток, в том числе и кератиноциты. Однако в настоящее время еще существуют сомнения в полной безопасности использования эмбриональных стволовых клеток для тканевой инженерии.
В. Терских, доктор биологических наук, Стволовые клетки, получение, хранение, возможности применения...
Дополнительная информация: |